Біологічно активні речовини (БАР) – це неорганічні ύ органічні
сполуки, загальною особливістю яких є висока активність у невеликих кількостях. Серед
біологічно активних речовин є як низькомолекулярні (наприклад, вітаміни,
алкалоїди), так і високомолекулярні сполуки (наприклад, ферменти, білкові
гормони). Загальною особливістю є висока активність у невеликих кількостях.
Більшість БАР відносять до продуктів вторинного обміну, вважаючи первинними
білки, ліпіди й вуглеводи. Вони не виконують ні будівельної, ні енергетичної
функції, а забезпечують зміну швидкості обміну речовин, пристосовуючи організм
до змін навколишнього середовища та здійснюють його захист від несприятливих
впливів. До біологічно активних речовин відносять ферменти, гормони,
фітогормони, вітаміни, фітонциди, алкалоїди, феромони, антибіотики та ін.
Історія дослідження.
Вітаміни.Існування і
значення вітамінів відкрив у 1880 році російський лікар М.Лунін, а польський
хімік К. Функ дав їм саме таку назву, бо вона містила у своїй молекулі
аміногрупу. Таким чином, вітаміни (лат. vita - життя і "амін" -
азотиста речовина, що містить NH2) - органічні сполуки різної хімічної природи,
необхідні для нормального обміну речовин, росту та розвитку, вони також
підвищують стійкість організму до захворювань. На сьогодні кількість відкритих
вітамінів сягає 30.
Гормони. Гормони були відкриті у 1905 році
Старлінгом і Бейлісом. Гормон - із грецької hormao – збуджую, тобто
вони є активатори, збудники різноманітних процесів у нашому організмі - і в
результаті цієї тонкої біохімії організм наш змінює свою поведінку - як на
фізичному, так і на психічному рівнях.
Ферменти. Фізіолог,
нобелівський лауреат І.П. Павлов назвав ферменти носіями життя. Ферменти
грають найважливішу роль переважають у всіх процесах життєдіяльності,
скеровуючи й регулюючи обмін речовин організму. Ферменти або ензими - органічні
каталізатори білкової або РНК природи.
Лабораторне дослідження
Виявлення наявності ферментів, що розщеплюють перекис водню
Основні групи біологічно активних речовин
Назва групи
|
Біологічне значення
|
Приклади представників
|
Ферменти
|
БАР, які здатні вибірково каталізувати певну біохімічну реакцію
|
Оксидоредуктази, трансферази, гідролази, ліази, ізомерази, лігази
|
Вітаміни
|
БАР, які в невеликих кількостях
необхідні для забезпечення життєдіяльності організмів
|
Жиророзчинні (А, Е, К) та водорозчинні
(В, С)
|
Гормони
|
БАР, які утворюються спеціалізованими клітинами і здійснюють ендокринну
регуляцію функцій організму
|
Соматотропін, тироксин, адреналін, інсулін, глюкагон, андрогени,
естрогени
|
Фітогормони
|
БАР, які регулють ріст і розвиток
ВИЩИХ рослин і грибів, а також відіграють важливу роль у пристосуванні рослин
до мінливих умов середовища
|
Стимулятори (ауксини, гібереліни, цитокініни, брасини)
та інгібітори (абсцизова кислота, етилен, жасмонова кислота).
|
Алкалоїди
|
БАР рослинного походження, які відіграють роль каталізаторів і завдяки
токсичності захищають рослини від поїдання
|
Хінін, кофеїн, нікотин, морфін, кокаїн, атропін, ефедрин, теобромін,
стрихнін, колхіцин
|
Фітонциди
|
БАР вищих рослин, які здатні вбивати
або пригнічувати ріст бактерій, грибів, найпростіших, забезпечуючи природний
імунітет
|
Аліцин цибулевих, гексенал грецького
горіха, хлорогенова кислота моркви і картоплі
|
Феромони
|
БАР тварин, що виділяються в довкілля і специфічно впливають на
поведінку, фізіологічні процеси і метаболізм інших особин того самого виду
|
Статеві феромони комах, феромони "тривоги" у риб
|
Антибіотики
|
БАР мікробного, рослинного і
тваринного походження, які вибірково пригнічують ріст мікроорганізмів, а
також клітин злоякісних пухлин
|
Стрептоміцин зі стрептоміцетів,
пеніцилін зі грибів, новоіманін зі звіробою, лізоцим зі слини.
|
Тема №5 Штучні і синтетичні волокна.
Визначення волокон за продуктами спалювання
Визначення волокон за продуктами спалювання
Штучні волокна, їх характеристика
Штучні волокна — волокна, які одержують з продуктів хімічної
переробки природних полімерів.
Віскозні волокна - це волокна з лужного розчину ксантогената. За
своєю будовою віскозне волокно нерівномірно: зовнішня його оболонка має кращу
орієнтацію макромолекул, ніж внутрішня, де вони розташовуються хаотично.
Віскозне волокно являє собою циліндр з поздовжніми штрихами, що утворюються при
нерівномірному твердінні прядильного розчину. Віскозне волокно володіє хорошою
гігроскопічністю (35-40%), світлостійкістю і м'якістю. Віскозне волокно
застосовується при виробництві тканин для одягу, білизняного та верхнього
трикотажу, як у чистому вигляді, так і в суміші з іншими волокнами і нитками.
Полінозне волокно - це модифіковане віскозне волокно. За
властивостями воно наближається до бавовни. Полінозне волокно відрізняється
однорідною структурою поперечного перерізу, має більшу, ніж віскозне волокно
міцність. Волокно має підвищену пружністю. Область використання його аналогічна
віскозному.
Ацетатне і триацетатні
волокна за своєю будовою аналогічні віскозному, але мають більші борозенки
вздовж волокна. Міцність ацетатного волокна нижче віскозного. Зазначені волокна
достатньо пружні, відрізняються стійкістю до дії мікроорганізмів, світлостійкі,
мають діелектричні властивості. Область їх використання аналогічна галузі
використання віскозного волокна.
Синтетичні волокна,
їх характеристика
Синтетичне волокно — це хімічне волокно, яке формують із синтетичних
полімерів. У промисловості для одержання синтетичних волокон застосовують
поліаміди,поліефіри,поліакрилонітрил,поліолефіни,полівінілхлорид,полівініловий
спирт.
Поліамідні волокна - капрон, анід, енант - найбільш широко
поширені. Початковою сировиною для нього є продукти переробки кам'яного вугілля
чи нафти - бензол і фенол. Волокна мають циліндричну форму, поперечний переріз
їх залежить від форми отвору філери, через яке продавлюються полімери.
Поліамідні волокна відрізняються високою міцністю при розтягуванні, стійкі до
стирання, багаторазовому вигину, володіють високою хімічною стійкістю,
морозостійкістю, стійкістю до дії мікроорганізмів. Основними їх недоліками є
низька гігроскопічність і світлостійкість, висока здатність наелектризовуватись
і мала термостійкість. Поліамідні волокна і нитки широко використовуються при
виробленні панчішно-шкарпеткових та трикотажних виробів, швейних ниток,
галантерейних виробів (тасьми, стрічки), мережив, канатів, рибальських сіток,
конвеєрних стрічок, корду, тканин технічного призначення, а також при
виробленні тканин побутового призначення в суміші з іншими волокнами і нитками.
Поліестер - лавсан, виробляються із продуктів переробки
нафти. У поперечному перерізі лавсан має форму кола. Одним з характерних
властивостей лавсану є його висока пружність, при подовженні до 8% деформації
повністю оборотні. На відміну від капрону лавсан руйнується при дії на нього
кислот і лугів, гігроскопічність його нижче, ніж капрону (0,4%), тому для
вироблення тканин побутового призначення лавсан в чистому вигляді не
застосовується. Волокно є термостійким, має низьку теплопровідність і великою
пружністю, що дозволяє отримувати з нього вироби, добре зберігають форму; мають
малу усадку. Недоліками волокна є його підвищена жорсткість, здатність до
утворення скатувань на поверхні виробів
і сильна здатність наелектризовуватись. Лавсан широко застосовується при
виробленні тканин побутового призначення в суміші з вовною, бавовною, льоном і
віскозним волокном, що надає виробам підвищену стійкість до стирання і
пружність. Він також з успіхом застосовується при виробництві нетканих полотен,
швейних ниток, гардинно-тюлевих виробів, технічних тканин і корду. Крім того,
волокно використовується в медицині для виготовлення хірургічних ниток і
кровоносних судин.
Поліакрилонітрильне
волокно-нітрон. Поліакрилонітрильні волокна виробляються з акрилонітрилу -
продукту переробки кам'яного вугілля, нафти чи газу. Акрилонітрил
полімеризацією перетворюється на поліакрилонітрил, з розчину якого формується
волокно. Потім волокна витягають, промивають, замаслюють, гофрують і сушать. Волокна
виробляються у вигляді довгих ниток і штапель. За зовнішнім виглядом і на дотик
довгі волокна схожі на натуральний шовк, а штапельні - на натуральну вовну.
Вироби з цього волокна після прання повністю зберігають форму, не вимагають
прасування. Волокно нітрон має низку цінних властивостей: по теплозахисних
властивостях воно перевершує шерсть, має низьку гігроскопічність (1,5%), м'якше
і шовковистою капрону і лавсану, стійко до дії мінеральних кислот, лугів,
органічних розчинників, бактерій, цвілі, молі, ядерним випромінюванням .
Використовується нітрон при виробництві верхнього трикотажу, платтяних тканин,
а також хутра на трикотажній і тканинній основі, килимових виробів, ковдр і
тканин технічного призначення.
Поліуретанові
волокно - спандекс. Волокно, що володіє низькою
гігроскопічністю. Особливістю всіх поліуретанових волокон є їх висока
еластичність - розривне подовження їх досягає 800%, частка пружною і еластичною
деформації - 92-98%. Саме ця особливість і визначає сферу їх використання. Спандекс
застосовується в основному при виготовленні еластичних виробів. З використанням
цього волокна виробляють тканини та трикотажні полотна для предметів жіночого
туалету, спортивного одягу, а також панчішно-шкарпеткові вироби.
Кевла́р (англ. Kevlar®) — торгова назва араміду (поліпарафенілен-терефталаміду), синтетичного волокна, що має високу міцність (у п'ять разів міцніше від сталі, границя міцності σв = 3620 МПа). Вперше кевлар було отримано
групою Стефані Кволек у 1964 в американській компанії DuPont, технологія виробництва розроблена цією ж компанією у 1965 році, з початку 1970-x років розпочато його комерційне
застосування.
Тема №4. Каучук.Гума.
Історія каучука.
Каучуки — полімери
рослинного або синтетичного походження, з яких виготовляють гуму. Характерна
властивість каучуків — висока еластичність, тобто здатність після деформації
відновлювати свою форму. Однак при нагріванні або охолодженні нижче -50 °С вони
втрачають цю властивість. Каучуки водонепроникні, зносостійкі, мають хороші
електроізоляційні властивості. Розрізняють природний і синтетичні
каучуки.Природний (натуральний) каучук міститься в соку деяких рослин. Цей сік
нагадує молоко і є емульсією каучуку у воді.Основу натурального каучуку
становить поліізопрен. У макромолекулі цього полімеру групи СН2 розміщені
з одного боку від подвійного зв’язку:

 Натуральний каучук
має білий колір; він легший за воду, розчиняється в бензині, бензені, деяких
інших органічних розчинниках. Полімер повільно окиснюється киснем повітря. Щоб
запобігти окисненню каучуку, щойно добутого із соку рослини, і розмноженню в
ньому бактерій, його обробляють розбавленими розчинами кислот (мурашиної,
оцтової) або інших речовин, промивають водою і висушують. У результаті каучук
набуває жовтуватого кольору. Серед усіх природних високомолекулярних сполук лише
каучук виявляє високу еластичність. Така властивість каучуку зумовлена
можливістю згортання його лінійних макромолекул у клубки. Якщо пластинку із
каучуку розтягувати, то макромолекули випрямляються, а якщо після цього
«відпустити», то вони повернуться в попередній стан, і пластинка набуде
початкової довжини. Доклавши більшого зусилля, каучукову пластинку можна
розірвати.
Натуральний каучук
має білий колір; він легший за воду, розчиняється в бензині, бензені, деяких
інших органічних розчинниках. Полімер повільно окиснюється киснем повітря. Щоб
запобігти окисненню каучуку, щойно добутого із соку рослини, і розмноженню в
ньому бактерій, його обробляють розбавленими розчинами кислот (мурашиної,
оцтової) або інших речовин, промивають водою і висушують. У результаті каучук
набуває жовтуватого кольору. Серед усіх природних високомолекулярних сполук лише
каучук виявляє високу еластичність. Така властивість каучуку зумовлена
можливістю згортання його лінійних макромолекул у клубки. Якщо пластинку із
каучуку розтягувати, то макромолекули випрямляються, а якщо після цього
«відпустити», то вони повернуться в попередній стан, і пластинка набуде
початкової довжини. Доклавши більшого зусилля, каучукову пластинку можна
розірвати.
Синтетичні каучуки. Натуральний каучук добувають у
значній кількості, проте цього недостатньо для задоволення зростаючих потреб.
Тому вчені створили синтетичні каучуки, які успішно замінюють природний каучук
і широко застосовуються в різних сферах.Більшість каучуків походить від
вуглеводнів із двома подвійними зв’язками в молекулі . Залежно від мономера
розрізняють бутадієновий каучук, ізопреновий (аналог натурального),
хлоропреновий та ін. Їх добувають, здійснюючи реакції полімеризації, переважно
за участю каталізаторів.Загальна схема утворення каучуків:
Бутадієн стирольний
каучук — продукт полімеризації двох сполук-мономерів.
Хімічні властивості. Маючи
подвійні зв’язки в макромолекулах, натуральний і синтетичні каучуки здатні
приєднувати водень, галогени, галогеноводні. При нагріванні за відсутності
повітря ці полімери розкладаються з утворенням відповідних мономерів.Каучуки
слугують сировиною для виробництва гуми і гумових виробів.Гума. Найеластичнішим
матеріалом серед природних і синтетичних матеріалів є гума. Її у великих
кількостях використовують для виготовлення шин Основу технології виробництва
гуми становить процес вулканізації, що полягає в нагріванні каучуку із сіркою.
Спочатку каучук змішують із наповнювачами (глиною, сажею, крейдою,
кремнеземом), барвниками і речовинами, які збільшують термін використання гуми.
Потім до суміші додають певну кількість сірки. У результаті взаємодії каучуку
із сіркою за рахунок розриву одного зі складників подвійного зв’язку
відбувається зшивання карбонових ланцюгів за допомогою «містків» -S-S- (мал.
97). При цьому частина подвійних зв’язків у макромолекулі залишається.
 Якщо взяти надлишок
сірки, то всі подвійні зв’язки будуть «витрачені» на зшивання карбонових
ланцюгів, і утвориться твердий термореактивний матеріал — ебоніт (мал. 98).
Його використовують для виготовлення електротехнічних деталей, хімічної
апаратури.Існують гуми різного призначення — для експлуатації при високих або
низьких температурах (тепло-, морозостійкі), для тривалого контакту з бензином
і нафтою (шланги на автозаправних станціях), кислотами і лугами, стійкі до
рентгенівського випромінювання тощо. Порівняння властивостей каучуків і
гуми. Каучук є еластичною речовиною, а гума — еластичним матеріалом. Каучуки
і гума не розчиняються у воді.
Якщо взяти надлишок
сірки, то всі подвійні зв’язки будуть «витрачені» на зшивання карбонових
ланцюгів, і утвориться твердий термореактивний матеріал — ебоніт (мал. 98).
Його використовують для виготовлення електротехнічних деталей, хімічної
апаратури.Існують гуми різного призначення — для експлуатації при високих або
низьких температурах (тепло-, морозостійкі), для тривалого контакту з бензином
і нафтою (шланги на автозаправних станціях), кислотами і лугами, стійкі до
рентгенівського випромінювання тощо. Порівняння властивостей каучуків і
гуми. Каучук є еластичною речовиною, а гума — еластичним матеріалом. Каучуки
і гума не розчиняються у воді.
Якщо ж помістити подрібнені шматочки каучуку і
гуми в органічний розчинник (бензен), то через добу каучук розчиниться з
утворенням колоїдного розчину, а гума лише збільшиться в об’ємі (набрякне). Це
свідчить про здатність гуми вбирати органічний розчинник. Каучук завдяки
наявності в ньому подвійних зв’язків може реагувати з галогенами. Зокрема, його
колоїдний розчин у бензені знебарвлює бромну воду. При нагріванні каучуки
розкладаються з утворенням ненасичених сполук. Наявність Сульфуру в гумі можна
довести, нагріваючи її в пробірці з газовивідною трубкою, зануреною в блакитний
розчин купрум(ІІ) нітрату. Сірководень, що є одним із продуктів термічного
розкладу гуми, спричинить утворення в розчині чорного осаду CuS. Працюючи в
хімічній лабораторії, потрібно враховувати, що гумові вироби (пробки, трубки)
руйнуються нітратною і концентрованою сульфатною кислотами. Розбавлені хлоридна
кислота і розчини лугів на гуму практично не діють.
Застосування каучуків і
гуми. Синтетичний ізопреновий каучук за властивостями схожий на
натуральний. Вироблена з нього гума вирізняється високою міцністю та
еластичністю. Цей каучук використовують у виробництві шин, конвеєрних доріжок,
взуття, медичних і спортивних виробів, ізоляційних матеріалів. Хлоропреновий
каучук є негорючим, термо- і світлостійким, не руйнується мастилами, не
окиснюється на повітрі. З нього виготовляють гуму для устаткування, що
контактує з нафтою і нафтопродуктами. Каучуки, які містять Флуор, хімічно
стійкі, витримують нагрівання до 300 °С.. Основне застосування гуми —
виробництво шин. Гумові вироби використовують у промисловості, техніці,
медицині, побуті.
Відходи гуми і довкілля. Майже 90 % від маси
гумових відходів припадає на зношені автомобільні шини, а решта — використані
предмети технічного та побутового призначення, старе взуття. У Європі
утилізують менше половини шин, непридатних для використання. Відходи гуми, як і
пластмас, не руйнуються в природних умовах. На жаль, більша частина їх
потрапляє в навколишнє середовище. Утилізацію гумових відходів здійснюють
спалюванням (після подрібнення) і термічним розкладом у спеціальних агрегатах1.
У першому випадку отримують теплову енергію (теплота згоряння гуми приблизно
така сама, що й вугілля), а у другому — добувають мономери для виробництва
каучуку.При спалюванні гуми на повітрі утворюється багато токсичних речовин. Гумові
відходи також використовують як поглиначі при очищенні стічних вод, у
виробництві ізоляційних матеріалів, будівництві, шляховому господарстві тощо.
ВИСНОВКИ
Каучуки — полімери, з яких виготовляють гуму та гумові вироби. Характерна
властивість каучуків — еластичність, тобто здатність після деформації
відновлювати свою форму. Більшість каучуків є полімерами вуглеводнів із двома
подвійними зв’язками в молекулах. Розрізняють натуральний і синтетичні каучуки.
Гума — продукт вулканізації каучуку. Цей еластичний матеріал широко
використовують у багатьох сферах. Утилізація гумових відходів є одним із
важливих екологічних завдань.
Тема №3.(опрацювання 08.04.2020-14.04.2020)
Полімери. Реакції полімерізації та поліконденсації.
Трохи історії.
Термін “полімерія” був введений
у науку І.Берцеліусом у 1833 для позначення особливого виду ізомерії, при якій
речовини (полімери), що мають однаковий склад, володіють різною молекулярною
масою, наприклад етилен і бутилен, кисень і озон. Такий зміст терміна не
відповідало сучасним представленням про полімери.
Ряд полімерів був, очевидно, отриманий ще в першій
половині 19 століття. Однак хіміки тоді звичайно намагалися придушити
полімеризацію і поліконденсацію, що вели до “осмоленню” продуктів основної
хімічної реакції, тобто, власне, до утворення полімерів (дотепер полімери
часто називають “смолами”). Перші згадування про синтетичні полімери
відносяться до 1838 (полівініліденхлорид) і 1839 (полістирол).
Хімія полімерів виникла тільки в зв’язку зі створенням
А.М.Бутлеров теорії хімічної будови. А.М.Бутлеров вивчав зв’язок між будівлею і
відносною стійкістю молекул, що виявляється в реакціях полімеризації. Подальший
свій розвиток наука про полімери одержала головним чином завдяки інтенсивним
пошукам способів синтезу каучуку, у яких брали участь найбільші
вчені багатьох країн (Г.Бушарда, У.Тілден, німецький учений До Гаррієс,
И.Л.Кондаків, С.В.Лебедєв і інші). У 30-х років було доведене існування
вільнорадикального й іонного механізмів полімеризації. Велику роль у розвитку
представлень про поліконденсацію зіграли роботи У.Карозерса.
Автором принципово нового представлення про полімери як
про речовини, що складаються з макромолекул, часток надзвичайно великої
молекулярної маси, був Г.Штаудингер. Перемога ідей цього вченого змусила
розглядати полімери як якісно новий об’єкт дослідження хімії і фізики.
Основні поняття.
Полімери (гр. polimeres – «багато частин») – це продукти
сполучення багатьох молекул в одну велику молекулу, внаслідок чого змінюються
властивості вихідного продукту.
Розмір молекули полімеру визначається ступенем
полімеризації n, тобто числом ланок у ланцюзі. Якщо n = 10…20, речовина
відноситься до легких масел. Зі зростанням n збільшується в'язкість, речовина
стає воскоподібною, нарешті, при n = 1000 утворюється твердий полімер. Ступінь
полімеризації необмежений: він може бути 104, і тоді довжина молекул досягає
мікрометрів. Молекулярна маса полімеру дорівнює добутку молекулярної маси
мономера та ступеня полімеризації. Молекули полімерів можуть мати лінійну,
розгалужену й зшиту будову. Це позначається на властивостях пластмас, зокрема,
зумовлює такі їх властивості, як термопластичність і термореактивнісь.
Термопластичні полімери – полімери, які після нагрівання і подальшого
охолодження зберігають свої властивості (поліетилен, поліпропілен, полістирол,
полівінілхлорид).
Термореактивні полімери – полімери, які після нагрівання і подальшого
охолодження втрачають пластичність та деякі інші властивості
(фенолформальдегідні смоли).
Властивості полімерів залежать від молекулярної маси,
хімічного складу й структури молекул.
Основними представниками полімерних матеріалів є пластмаси,
каучуки і волокна.
Полімеризація – процес послідовного сполучення молекул
низькомолекулярної речовини з утворенням високомолекулярної
Полімеризацією етилену і його гомологів добувають
поліетилен, поліпропілен та багато інших.
Поліконденсація – реакція утворення полімеру внаслідок взаємодії
функціональних груп молекул мономера, яка відбувається з виділенням води,
амоніаку або інших низькомолекулярних сполук
Поліконденсацією формаліну з карболовою кислотою
добувають карболіт.
Фенолформальдегідні смоли.
Утворення поліпептидного ланцюга
Поліетилентетрафталат матеріал тари для газованих напоїв та тканини,що не пропускає вологу.
Щоб надати полімеру потрібних властивостей і
перетворити їх на пластмасу у полімерну масу додають наступні компоненти:
- пластифікатори – для надання
еластичності і зниження крихкості;
- барвники, які надають
матеріалу потрібного забарвлення;
- антистатики для запобігання
накопиченню статичної електрики;
- наповнювачі (кварцове і деревне борошно, мелена крейда чи слюда, волокна, азот, повітря, папір) поліпшують механічні властивості й зменшують собівартість.
Застосування полімерів в Україні сьогодні.
Інтерактивний плакат Тефлон
Посилання на онлайн сервісТема №2. (опрацювання 31.03.2020-07.04.2020)
Амінокислоти.Білки.
1. Загальна характеристика амінокислот
 Амінокислоти — органічні сполуки, в молекулі яких
одночасно містяться дві функціональні групи: аміногрупа -NH2 і карбоксильна
група -СООН.
Амінокислоти — органічні сполуки, в молекулі яких
одночасно містяться дві функціональні групи: аміногрупа -NH2 і карбоксильна
група -СООН.
Білки складаються із залишків молекул амінокислот
сполучених пептидними зв'язками.
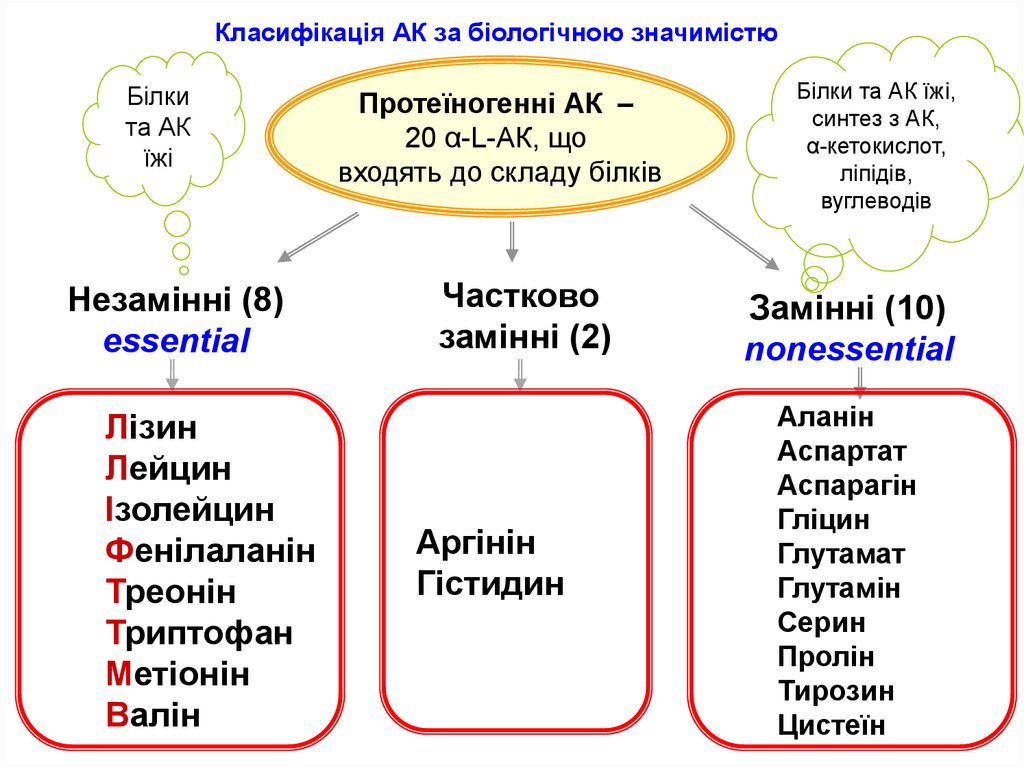
Двадцять амінокислот, з яких побудовані білки,
називають стандартними або протеїногенними амінокислотами.
У залежності від того, до якого атому Карбону
приєднана аміногрупа, амінокислоти поділяються на α-, β-, γ- тощо. У
α-амінокислотах карбоксильна група і аміногрупа приєднані до одного атома Карбону.
Усі протеїногенні амінокислоти є α-амінокислотами. Їх загальна формула:
2. Номенклатура амінокислот
За систематичною номенклатурою назви амінокислот
утворюються від назв відповідних карбонових кислот додаванням префікса аміно- і
номера атома, від якого відходить аміногрупа. Наприклад: 2-амінобутанова
кислота.
Для α-амінокислот, які входять до складу білків,
використовують тривіальні назви:

 Хімічні властивості аміноетанової кислоти
Хімічні властивості аміноетанової кислоти
За хімічними властивостями амінокислоти — органічні
амфотерні сполуки, які проявляють властивості як основ, так і кислот.
Осно́вні
властивості амінокислот пов'язані з наявністю в молекулі аміногрупи -NH2.
Кислотні властивості амінокислот пов'язані з
наявністю в молекулі карбоксильної групи -СООН
1. Як основи амінокислоти реагують з кислотами,
утворюючи солі:
NH2–СH2–СООН + HCl → NH3Cl–СH2–СООН - хлорид аміноетанової
кислоти
2. Як кислоти амінокислоти реагують з основами та
основними оксидами, утворюючи солі:
NH2–СH2–СООН + NaOH → NH2–СH2–СООNa + H2О - аміноацетат натрію.
3. Як кислоти
амінокислоти реагують з спиртами, утворюючи естери:
NH2–СH2–СООН +
СH3OH → NH2–СH2–СООСH3 + H2О -
метиламіноацетат
4. Амінокислоти
сполучаються з іншими амінокислотами, утворюючи пептиди. Зв'язок між залишками
амінокислот називається пептидним:
Пептиди — речовини, молекули яких побудовані із залишків α-амінокислот, з’єднаних між собою пептидними зв’язками.
Пептиди з великою молекулярною масою (більше 10 тисяч а.о.м., або більше 100 амінокислотних залишків) називають білками.
Утім, до білків відносять і інсулін, хоча його молекулярна маса лише біля 5,5 тисяч а.о.м. і він складається з 51 амінокислотного залишка.
Білки
Структура білків
- Первинна структура – послідовне лінійне сполучення залишків амінокислот, сполучених пептидними зв’язками
- Вторинна структура – спіраль, витки якої сполучені водневими зв’язками
- Третина структура – глобула або фібрила, зв’язки водневі, гідрофобні, йонні
- Четвертинна структура – поєднання кількох білкових молекул, зустрічається лише в частини білків. Найвідоміший білок з четвертинною будовою молекули — гемоглобін
Глобулярні білки (альбуміни) розчинні у воді, фібрилярні (колаген, кератин) – нерозчинні.
Хімічні властивості білків
Денатурація білка —
це руйнування четвертинної, третинної і вторинної структури білка. Вона може
бути викликана нагріванням, дією радіації, струшуванням. Денатурація білка
відбувається при варінні яєць, приготуванні їжі тощо.
Ренатурація — це
процес, оборотний денатурації, при якому білки, повертають свою третинну і
вторинну структуру.Денатурація — руйнування вищих рівнів структурної організації
білка – вторинной, третинної, четвертинної.
Денатурація буває оборотна і необоротна.
Оборотна денатурація
— від механічної дії, солей, слабких кислот.
Процес відновлення структури білка називається
ренатурація.
Необоротна денатурація — вплив високої температури,
концентрованих розчинів кислот, лугів, солей важких металів.
Кольорові реакції білків:
Біуретова реакція – синьо-фіолетове забарвлення з купрум (ІІ) гідроксидом.
Ксантопротеїнова реакція – жовте забарвлення під впливом концентрованої нітратної кислоти.
Гідроліз – розпад білка на амінокислоти. Відбувається під дією кислот та лугів при нагріванні. В організмі — в процесі травлення, під дією ферментів.
Значення білків для організмів.






















Немає коментарів :
Дописати коментар